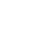
|
产品
|
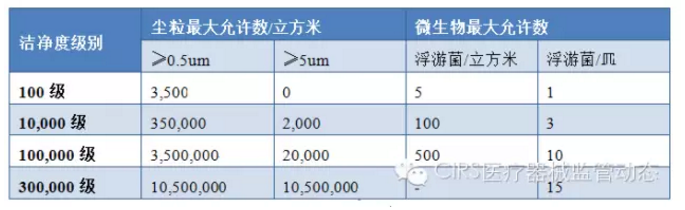
洁净度级别
|
|
植入和介入到血管的器械:如血管支架
不清洗零部件的加工;末道清洗及组装;处包装及其封口;等
|
不低于10,000级
|
|
植入到人体组织的器械:如起搏器,人工关节
不清洗零部件的加工;末道清洗及组装;初包装及其封口;等
|
不低于100,000级
|
|
与人体损伤表面和粘膜接触的器械:如溃疡敷料等
不清洗零部件的加工;末道清洗及组装;初包装及其封口;等
|
不低于300,000级
|
|
对有要求或无菌操作技术加工的,如血管支架涂药
|
在10,000级下局部100级洁净区内
|
|
注:
如果初包装材料不与器械直接相接触,可以在不低于300,000级下包装。
洁净工作服清洗、干燥和穿洁净工作服室、专用工位器具的末道清洗与消毒的区域的空气洁净度级别可低于生产区一个级别。
|
|
声明:本网站发布的内容(图片、视频和文字)以原创、转载和分享网络内容为主,如果涉及侵权请尽快告知,我们将会在第一时间删除。文章观点不代表本网站立场,如需处理请联系客服。电话:189-5653-9761。
本站全力支持关于《中华人民共和国广告法》实施的“极限化违禁词”的相关规定,且已竭力规避使用“违禁词”。故即日起凡本网站任意页面含有极限化“违禁词”介绍的文字或图片,一律非本网站主观意愿并即刻失效,不可用于客户任何行为的参考依据。凡访客访问本网站,均表示认同此条款!反馈邮箱:365667427@qq.com。
净化厂房装修_洁净室净化空调系统如何节能运行?
1、新风热、湿处理所消耗的能量根据国家规范的规定,由于卫生要求,洁净室内工作人员所需新风量,维持室内正压所需的新风量,系统的排风量,系统及洁净室的漏风量。这些新风量之和,对于10万洁净室则大于等于30%,1万级洁净室不低于20%,1000级洁净室则不低于1...
合肥净化工程_无尘室管理规定及制度条文说明
目录(Tableofcontent) 1.大纲(Introduction)1.1范围(Scope)1.2目的(Purpose)2.引用文件(Referencedocument)3.名词定义(Definition)4.无尘室管理规范程序4.1无尘室...
安徽洁净厂房净化工程_洁净厂房管理规范
1目的1.1为确保洁净厂房之环境,降低本公司管理成本,确保产品品质及提升经营效益。 2适用范围2.1凡是所有进入洁净厂房之人员(包括本公司人员,厂商及参观来宾等)及原材料等均接受本管理规则所约束规范。 3职责3.1制造部:负责对所有进入...
安徽净化厂房施工_电子厂房洁净室管理制度
1目的为维持洁净室内洁净度,管制污染源控制环境参数,特对于洁净室内之人、机器设备、物品、原物料等加以管制,以便能确保洁净室内洁净度符合产品制程之需求,提高产品品质。 2适用范围凡进入洁净室内所有人、机器设备、物品、原物料、产品等,均属...
安徽净化工程_无尘室管理规范版本大全
无尘室管理规范版本大全无尘室管理规范一一适用范围:凡进入无尘室之人员(包括本公司之人员,厂商及参观来宾等)均接受本管理规则所约束二目的:为确保无尘室的环境品质及降低本公司管理成本,确保产品品质及提升运营效益三内容:1、进入无尘室之管理1.1本公司人员进入无...
《洁净厂房施工综合技术》-郑玉柱全文完整版
前言郑玉柱洁净技术及玷污控制技术,实际上常用玷污控制(ContaminationControl)一词。其全面的概念应是:对加工或处理对象在加工处理过程中,由于玷污物质的存在,影响对象的成功率,而对到达对象表面的玷污物质进行控制后,能提高对象的成功率,此有效...


 客服微信
客服微信